化学者のつぶやき
がんをスナイプするフェロセン誘導体
![[写真]](pack/images/index_mainvisual_01.jpg)
がん細胞中で活性化されミトコンドリアへ集積するフェロセン誘導体が開発された。がん細胞選択的な医薬品開発やイメージングへ応用可能である。
がん細胞選択的に作用する抗がん剤
がんの治療技術はここ10年間で急速に進歩しているものの、化学療法に伴う副作用は未だ大きな問題である。そこで、ガン細胞に過剰に発現しているキナーゼタンパク質(1)や活性酸素種(ROS)濃度増加(図1A)(2)など、ガン細胞特有の性質が着目された。これらの特徴をターゲットにした抗がん剤は、がん細胞特異的に作用し副作用を軽減できるため、患者のQOL向上の面などから需要は大きい。
その中でもミトコンドリアは遺伝子の発現調整や代謝制御などの重要な機能を有しているため、新たながん選択的な抗がん剤の標的として盛んに研究が行われている(3)。例えばがん細胞のミトコンドリアの膜電位は通常細胞よりも負に分極しているため(図1A)、カチオン種(脂溶性カチオン種; DLCs)がミトコンドリアに集積しやすい。これを利用したがん選択的抗がん剤としてR123(1)(4)やMKT-077(2)(5)のようなDLCsが有効と考えられたが、いずれも副作用および薬効の低さから実用化に至っていない(図1B)。
今回MokhirらはROSによりDLCsを発生させるハイブリッド戦略により、がん細胞選択的な抗がん活性を有するフェロセン誘導体3の開発に成功した(図1C)。すなわち、3は細胞内でROSによりDLCs3’に変換された後、ミトコンドリア内に移行し活性を示す。がん細胞特有の高濃度ROSにより3の生成ががん細胞内選択的に起こるのに加え、ミトコンドリアの膜電位差(ΔΨC)が大きいためミトコンドリア選択性も高い。このようにして3はがん細胞高選択的に働くことができる。
がん細胞特有の性質 (B) 抗がん活性を有するDLCs (C) ROSおよびDLCsを利用したがん選択的抗がん剤](pack/images/index_img_01.jpg)
図1. (A)がん細胞特有の性質 (B) 抗がん活性を有するDLCs (C) ROSおよびDLCsを利用したがん選択的抗がん剤
“
“ROS-Responsive N-Alkylaminoferrocenes for Cancer-Cell-Specific Targeting of Mitochondria”
Reshetnikov, V.; Daum, S.; Janko, C.; Karawacka, W.; Tietze, R.; Alexiou, C.; Paryzhak, S.; Dumych, T.;
Bilyy, R.; Tripal, P.; Schmid, B.; Palmisano, R.; Mokhir, A. Angew. Chem., Int. Ed. 2018, Early View![]() . DOI: 10.1002/anie.201805955
. DOI: 10.1002/anie.201805955![]()
”
論文著者の紹介
![[写真]](pack/images/index_img_02.jpg)
研究者:Andriy Mokhir![]()
研究者の経歴:
-1995 BSc, Taras Shevchenko National University of Kyiv, Ukraine
-1997 Ph. D, Taras Shevchenko National University of Kyiv, Ukraine
1997-2001 Posdoc, North Dakota State University, USA (Prof. Kenton Rodgers); Tufts University, USA (Prof. Clemens. Richert); Heidelberg University, Germany (Prof. Roland Kramer)
2002-2010 Group Leader at Heidelberg University
2011-2012 Guest Prof. at Wien University, Austria
2012-2013 Prof. (W2) at Heidelberg University, Germany
2013- Prof. (W2) at Friedrich Alexander University Erlangen-Nuremberg, Germany
研究内容:ケミカルバイオロジー、創薬化学
論文の概要
著者らはまずフェロセン誘導体ががん細胞のミトコンドリアに集積するかを確認するため、誘導体4を合成した。4自身はフェロセン–蛍光部位間での光誘起電子移動のため蛍光を示さないが、ROSにより4が活性されて生成する4’は蛍光を示す。1のようなローダミン誘導体のミトコンドリア標識剤と4をがん細胞(A2780)および通常細胞(NHDF)に投与し蛍光を確認したところ、A2780ではCh2が確認されたのに加え、Ch1とCh2の蛍光部位が一致した。一方NHDFではCh2が現れなかった。以上より4はがん細胞中でのみROSによって4’へ変換され、DLCsによりミトコンドリアに集積すると判明した(図2A)。
この知見よりフェロセンユニットが抗がん剤のキャリアーに応用できると予測された。そこで、カルボプラチンとフェロセンユニットを組み合わせたフェロセン誘導体5を合成した。その後、5、カルボプラチン誘導体6とシスプラチン(7)を、A2780、シスプラチン耐性A2780(A2780cis)およびNHDFへ投与して活性評価を行った。A2780では5は6よりも高い活性を示したことから、フェロセンユニットが抗がん剤の活性を高めていると判明した(図2B Table 1)。5を投与した場合、6の場合よりミトコンドリアに含まれるPtの割合が大きいこともこの結果を支持する(図2B Figure 1)。また、A2780cisに5と7を投与した場合、7の活性は低下したが、5はA2780の場合と同等の活性を維持しており、5がシスプラチン耐性型にも有効であるとわかった(図2B Table 2)。さらに、5はNHDFにおいて毒性を示さず、副作用の少ない抗がん剤となりうる可能性を示唆している(図2B Table 3)。
以上、がん選択的な染色および殺傷が可能なフェロセン誘導体が開発された。がんの治療や診断への応用が期待される。
 ミトコンドリアのイメージング (B) 活性評価 (図 論文より引用、一部改変)](pack/images/index_img_03.jpg)
図2. (A) ミトコンドリアのイメージング (B) 活性評価 (図 論文より引用、一部改変)
参考文献
- Wiestner, A. Blood,2012, 120, 4684. DOI: 1182/blood-2012-05-423194<
 .
. - Reshetnikov, V.; Daum, S.; Mokhir, A. Chem Eur. J. 2017, 23, 5678. DOI:10.1002/chem.201701192
 .
. - Vander Heiden, M. G.; DeBerardinis, R. J. Cell 2017, 168, 657. DOI: 1016/j.cell. 2016.12.039
 .
. - Modica-Napolitano, J. S.; Aprille, J. R. Cancer Res.1987, 47, 4361. (LINK
 )
) - Britten, C, D.; Rowinsky, E. K.; Baker, S. D.; Weiss, G. R.; Smith, L.; Stephenson, J.; Rothenberg, M.; Smetzer, L.; Cramer, J.; Collins, W.; Von Hoff, D. D.; Eckhardt, S. G. Clin. Cancer Res.2000, 6, 42. ((LINK
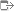 )
)